研究紹介
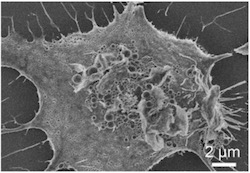
薬物送達システム(DDS)は薬物を必要な場所に、必要な量を、特定の時間作用させる技術で、薬効の増強、副作用の軽減、そして、経済性の向上が期待されます。私たちは、生分解性ポリマーナノ粒子やシリカナノ粒子、金ナノ粒子を使い、特性の細胞へ薬物を送達する技術に関する研究をしています。特に、標的細胞としてマクロファージに注目し、そして、新たな抗炎症作用を持つ化合物の探索も行いながら、様々な炎症性疾患の新たな治療法を開発しています。

https://doi.org/10.1016/j.jddst.2023.104981(ポリ乳酸ナノ粒子による抗炎症剤のクッパー細胞へのデリバリーと肝炎治療に関する研究)
https://doi.org/10.1246/bcsj.20210064(金ナノ粒子の発光特性に関する研究)
https://doi.org/10.1021/acsomega.0c05162(金ナノロッド表面構造と細胞内取り込み経路に関する論文)
https://link.springer.com/article/10.1007/s00380-018-1241-2(金ナノロッドの心不全心筋への蓄積に関する研究)
銀ナノ粒子は強い抗菌活性を持ちますが、細胞毒性も無視できないため、抗生物質として利用は難しく、そこで、必要な時に、必要な場所で作用させることができれば、新たな感染症治療薬として利用できると期待されます。私たちは銀ナノ粒子を金やシリカ、あるいは、生分解性ポリマーでコートし、抗菌活性をあえて低下させ、しかし、そこに光を照射することで、銀ナノ粒子の構造を変化させ、抗菌活性を高める技術について研究しています。そして、その技術を結核や肺MAC症といった細胞内寄生菌による難治感染症の治療に利用できないかと考えています。

https://doi.org/10.1093/chemle/upae084(ポリ乳酸ナノ粒子に銀ナノ粒に内包させ、細胞内寄生菌を殺菌する研究)
https://doi.org/10.1021/acsabm.3c00019(細菌毒素タンパク質を銀ナノ粒子に修飾し、細胞内寄生菌を殺菌する研究)
https://doi.org/10.1021/acsomega.1c07058(シリカコート銀ナノプレートの光照射による抗菌活性制御)
https://doi.org/10.1246/bcsj.20180232(銀ナノ粒子を金原子コートすることによる抗菌活性の促進)
https://doi.org/10.1021/acs.langmuir.8b00540(銀ナノ粒子を金原子コートすることによる分散安定性向上と細胞内寄生菌傷害)
https://doi.org/10.1246/cl.171022(銀ナノプレートの抗バイオフィルム活性)
https://doi.org/10.1039/c7nr06513b(金原子コート銀ナノプレートの光照射による抗菌活性制御)
グラフェン量子ドットはナノサイズのグラフェンで蛍光を発したり、抗菌・抗ウイルス活性をもち、新たな医療材料として期待されています。私たちは独自の合成方法を見出し、その生成機構の解明から、医療材料としての応用まで幅広く研究を進めています。

シルクフィブロインはカイコが産生する繊維タンパク質で絹糸の主要成分です。 私たちはこれをスポンジやフィルム、チューブ、マイクロ粒子など様々な形状に加工し、医療材料として応用する研究を進めています 。「あつまる新シルク蚕業開発共同研究分野」

https://doi.org/10.1021/acsabm.9b00957(マグネシウム合金製ステントのシルクフィブロインによる表面コーティング)
マグネシウム合金は水中で腐食されやすく、その腐食性をコントロールすることで生体吸収性の医療材料として利用できます。私たちは、マグネシウム合金の表面修飾による腐食速度のコントロールに成功し、それを様々な医療機器へ応用する研究を進めています。

https://doi.org/10.3390/pharmaceutics14030492(薬物放出ステントに関する総説)
https://doi.org/10.3390/ma15093132(マグネシウム合金製ステントのパリレンCによる表面コーティングと腐食耐性向上)
https://doi.org/10.3390/pharmaceutics14030492(冠動脈ステントからのシロリムス放出に関する総説)
https://doi.org/10.1021/acsabm.9b00957(マグネシウム合金製ステントのシルクフィブロインによる表面コーティング)
https://doi.org/10.1016/j.colsurfb.2017.12.032(マグネシウム合金製ステントのポリマーコーティングと腐食耐性向上)
がん組織への薬物送達には脂質ナノ粒子、ポリマーナノ粒子なの様々な材料が使われています。また、がん組織の微小環境を認識し、そこへ留まり、薬物を放出する技術は、がんの診断や治療を支える重要な技術となります。私たちは脂質ナノ粒子やポリマーナノ粒子、またこれらのハイブリッドナノ粒子にがんを認識し、応答するペプチドを組み合わせ、高精度かつ高効率ながんの診断や治療を行うナノシステムを開発しています。
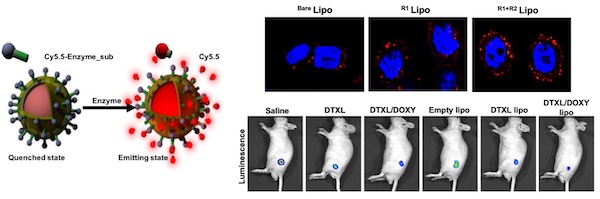
https://doi.org/10.1016/j.jconrel.2020.12.011(pH応答型リポソームによる非小細胞肺癌治療に関する研究)
https://doi.org/10.3390/pharmaceutics12060585(ErbB2を標的にしたリポソームによる乳がん細胞への薬物送達)
https://doi.org/10.3389/fbioe.2020.00133(金ナノスターを用いたがん治療に関する研究)
自省を込めて毎日日記をつけています。
鹿児島で生まれ、すくすく育つ、そして、、、
1994年3月 九州大学大学院理学研究科化学専攻博士課程 修了
1994年3月 博士(理学)取得
1994年4月 長崎大学工学部応用化学科 助手
2001年8月〜2002年7月 文部科学省在外研究員(米国ピッツバーグ大学薬学部)
2003年4月 長崎大学大学院生産科学研究科 助手
2004年4月 九州大学大学院工学研究院応用化学部門 助教授
2007年4月 九州大学大学院工学研究院応用化学部門 准教授
2012年12月 熊本大学大学院自然科学研究科 産業創造工学専攻 物質生命化学講座 教授
2016年4月 熊本大学大学院先端科学研究部 生体関連材料分野 教授
現在に至る
日本化学会、高分子学会、日本生化学会、日本ペプチド学会、日本DDS学会、コントロールドリリース学会、日本バイオマテリアル学会、遺伝子・デリバリー研究会